Wei Chi instrument
Your laboratory is always a good helper
自然杀伤(NK)细胞是起源于淋巴的细胞毒性先天免疫细胞。1973年,人们发现了一种非T非B淋巴细胞亚群可有效杀死被抗体识别的细胞,随后首次被描述为“null”杀伤细胞。两年后,有报道称这种细胞能够杀死各种类型的肿瘤细胞,并创造了术语“自然”杀伤细胞。NK细胞不仅在抗肿瘤反应中发挥作用,而且在抵抗微生物感染方面也发挥作用。
NK细胞表达多种激活和抑制受体,这些受体介导的信号之间的平衡决定了NK细胞激活的结果。NK细胞在没有预先致敏的情况下杀死癌细胞的能力在肿瘤免疫监测中发挥重要作用。以 NK 细胞为基础的肿瘤免疫治疗领域已经到了一个激动人心的关头。虽然这些疗法还没有取得与过继性 T 细胞疗法同样程度的临床成功,但是早期的令人鼓舞的结果使 NK 细胞疗法的开发热情越来越高。
NK细胞生物学
NK细胞是个被鉴定的先天性淋巴细胞(ILC)亚型,能对病毒感染和/或转化的细胞产生多种效应器功能,主要是细胞杀伤和产生促炎细胞因子。NK细胞和其他ILC家族成员(—1型ILC(ILC1s)、ILC2s和ILC3s)与B细胞和T细胞来源于相同的淋巴祖细胞。NK细胞的细胞毒性活性使它们在功能上与CD8+T细胞为相似,而ILC1、ILC2和ILC3群体的细胞因子生成模式将这些细胞分别对应CD4+T细胞的TH1、TH2和TH17亚群。
NK细胞的两个典型的亚群是CD56brightCD16-和CD56dimCD16+群体。CD56bright细胞在外周血中的数量较少(循环中90%的NK细胞是CD56dim),而组织中的NK细胞主要是CD56bright。CD56bright NK细胞是强有力的细胞因子产生者,除非受到促炎性细胞因子如IL-15的刺激,否则细胞毒性较弱。相比之下,CD56dim NK细胞群可介导感染细胞和恶性细胞的连续杀伤,主要通过包含颗粒酶B和穿孔素的预先组装的溶细胞颗粒在免疫突触中的胞吐,终诱导靶细胞凋亡。
NK细胞的抗肿瘤效应机制
NK细胞具有多种功能,可以限制癌细胞的生长和扩散。在TME先天性和适应性免疫细胞产生促炎性趋化因子的指导下,循环NK细胞可被招募到肿瘤发生的部位。CXCR3–CXCR4、CX3CR1和CCR3–CCR5是NK细胞亚群差异表达的主要趋化受体。
进入TME后,NK细胞可以通过“丢失自我”机制杀死癌细胞。许多癌细胞下调MHC I分子的表达,以逃避细胞毒性CD8+T细胞的检测,然而NK细胞能够识别和响应这种缺失的自我表型的细胞,终导致靶细胞裂解。因此,在T细胞不能识别MHC I下调癌细胞的情况下,NK细胞具有治疗潜力。
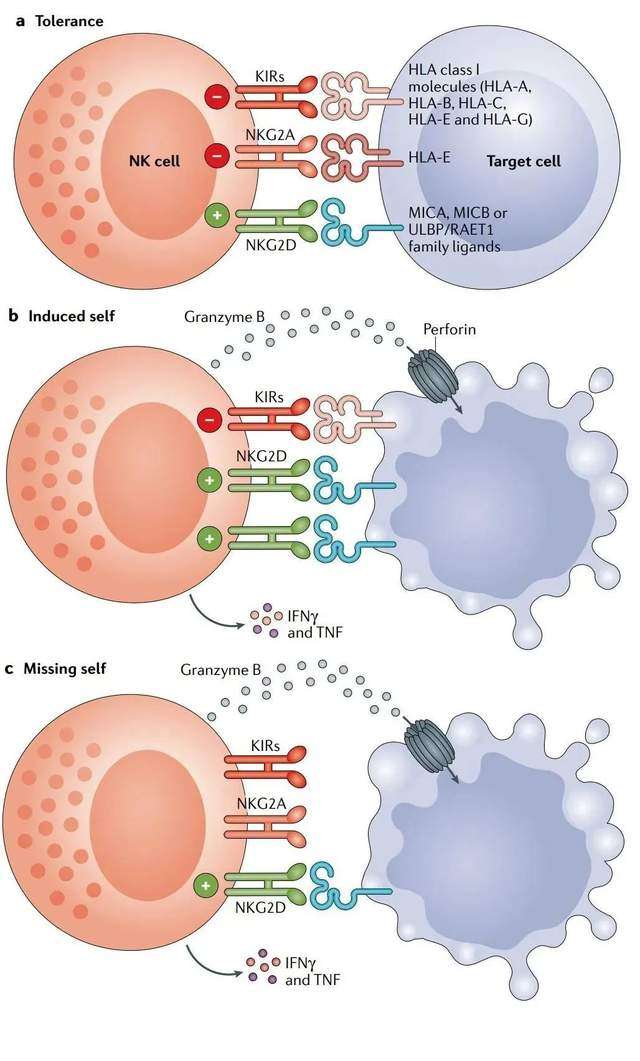
ADCC是NK细胞介导的杀伤癌细胞的另一个关键机制。除了直接诱导细胞毒性外,NK细胞还通过产生促炎性细胞因子(包括IFN-γ和TNF)对转化细胞作出反应。
NK细胞的免疫检查点抑制
关于ICI的研究主要集中在抗肿瘤T细胞的去抑制,这种治疗模式增强NK细胞的活性也引起了相当大的关注。例如,人源化抗NKG2A单克隆抗体monalizumab目前正在对多种癌症患者进行单药试验,或与其他免疫检查点抑制剂联合应用,临床前数据表明这种药物能显著增强NK细胞和T细胞的细胞毒性。
TIGIT是另一种由NK细胞和T细胞表达的抑制性受体,其配体在人类肿瘤浸润的NK细胞上过表达。在一些小鼠模型中,TIGIT抑制逆转NK细胞衰竭并促进NK细胞依赖性抗肿瘤免疫。已经设计了一些积的临床试验来测试单独抗TIGIT药物以及与其他免疫检查点抑制剂联合使用的有效性和/或安全性。(如NCT03119428、NCT04150965、NCT04047862、NCT04256421、NCT03563716和NCT04294810)
另外还有LAG-3和TIM-3,来自小鼠NK细胞研究的数据表明LAG-3在介导对肿瘤细胞系的细胞毒性方面起着积作用;肺腺癌患者NK细胞上TIM-3表达增加预示着不良预后,体外抑制这种NK细胞的TIM-3增强了其细胞毒性和IFNγ的产生。目前,多个临床试验正在对各种癌症患者进行LAG-3和TIM-3抑制剂的试验,(包括NCT01968109、NCT04150965、NCT04140500、NCT03625323、NCT0331142、NCT03066648、NCT03489343、NCT03680508和NCT04139902等)。
其它基于NK细胞的免疫检查点还包括CD96、 Siglec-7/9、CD200R、CD47、CTLA-4、PD-1和B7-H3,将这些检查点结合起来进行协同抗肿瘤反应是未来充分发挥NK细胞杀伤肿瘤作用的方向。
过继性NK细胞疗法
异基因外周血NK细胞只是治疗性NK细胞众多潜在来源之一。NK细胞约占外周血淋巴细胞总数的10%,而脐带血(UCB)中的NK细胞占淋巴细胞总数的30%;因此,UCB是治疗效应NK细胞的可靠来源。UCBNK细胞的治疗效果目前正在一些临床试验中进行评估(如NCT01619761和NCT02280525)。
克隆性NK细胞系,如NK-92、KHYG-1和YT细胞,是异基因NK细胞的替代来源,NK-92细胞系已在临床试验中得到广泛测试。然而,这些细胞是非整倍体,因此遗传不稳定,这就要求它们在输注前接受辐照。辐照的NK-92细胞被观察到可以杀死癌症患者的肿瘤细胞。
此外,临床上正在对来自多种来源的干细胞衍生NK细胞产物进行检测,包括来自UCB干细胞或诱导多能干细胞(IPSC)的NK细胞产物。将成年细胞重新编程为多能干细胞,以使其分化为NK细胞并扩展生成终产物,是基于iPSC的方法的一个独特特征。一项临床试验目前正在招募血液或实体癌患者,以测试这些现成的iPSC衍生NK细胞的安全性。
适应性NK细胞是治疗性NK细胞的另一个新兴来源。适应性NK细胞是一种自然发生的细胞群,在HCMV感染或再激活后在人类中扩增。HCMV UL40衍生肽抗原-HLA-E复合物与NK细胞上NKG2C之间的相互作用,导致NKG2ChiCD57+NK细胞增殖,NKG2ChiCD57+NK细胞下调参与细胞内信号传导的某些蛋白质,包括PLZF、SYK和FcεRIγ。适应性NK细胞具有一些独特的效应器特性,包括增强的ADCC、增强的细胞因子反应和对MDSCs和Treg细胞免疫抑制作用的固有抵抗。目前,三项临床试验正在评估这些适应性NK细胞对各种癌症患者的疗效。
细胞因子诱导记忆样(CIML)NK细胞是异基因细胞治疗的另一种选择,与其他类型的NK细胞产品相比具有独特的优势。CIML-NK细胞在体外通过IL-12、IL-15和IL-18的短暂启动,产生对细胞因子反应增强的NK细胞,并激活持续数周至数月的受体刺激。将这些CIML-NK细胞输注到携带AML异种移植物的小鼠体内可产生强大的抗肿瘤作用并显著延长存活时间。在I期试验中,CIML NK细胞具有良好的安全性,在44%的可评估AML患者(4/9)体内扩增并诱导病情缓解。
CAR-NK
嵌合抗原受体(CAR)是一种受体蛋白,它赋予免疫细胞新的能力,以靶向特定的抗原蛋白。CAR-NK细胞免疫疗法比CAR-T细胞免疫疗法更安全,而且NK细胞的安全性已在一些临床领域得到验证。例如,一些I/II期试验显示,同种异体NK细胞输注耐受性良好,不会引起GVHD和明显的毒性。因此,NK细胞是一种适应性更强的CAR载体,而不仅仅局限于自体细胞。
NK细胞上表达的功能性CAR分子由三部分组成:胞外结构域、跨膜区以及胞内的信号结构域。胞外结构域由一个信号肽和识别抗原的单链抗体片段(scFv)组成,一段铰链区将这个结构连接到跨膜区,它也在细胞内连接到包含激活信号的胞内结构域。成功的CAR设计是通过仔细的设计和功能测试相结合来实现的。
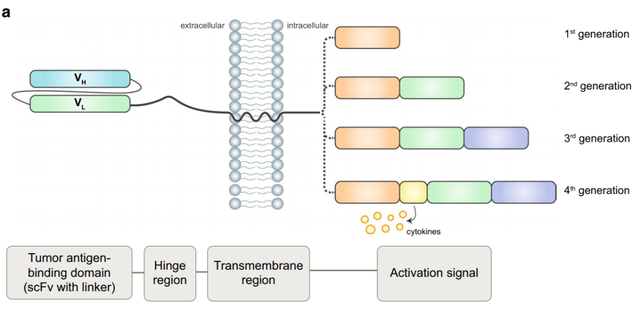
载体骨架和启动子
载体骨架包含表达CAR所需的所有元件,如启动子、polyA信号和转录调控片段。
启动子的选择直接影响到转基因的表达水平。目前,对不同启动子在NK细胞系中的CAR表达和功能的比较只有一次报道,而对原代NK细胞没有比较数据。就这一次单个报告来看,还不能确定CAR-NK细胞的佳启动子。
目前关于CAR-NK细胞的报道显示,多种启动子被用于驱动CAR的表达,无论是细胞系来源的还是原代NK细胞。在原代CAR-NK和CAR-NK细胞系中,病毒启动子(CMV、MPSV、MMLV、SFFV等)比组成性活性启动子(如EF1α、CMV和PGK)更常用。
信号肽
在信号肽中存在着巨大的异质性,这直接转化为不同水平的蛋白质分泌效率。对于CAR-NK和CAR-T细胞,还没有确定佳信号肽的比较研究。目前,CD8a-SP是原代NK细胞常用的信号肽序列(16%,71%的研究中未公布)和NK细胞系的免疫球蛋白重链或轻链信号肽(29%)。
单链抗体
单链抗体片段是CAR的肿瘤抗原结合域,该结构域将决定CAR-NK细胞的特异性和功能。
由于单链抗体不是抗体的天然形式,因此重链和轻链的顺序是人工确定的。到目前为止,对于CAR-NK设计,大多数更喜欢VH-VL方向,而不是VL-VH方向。
Fujiwara等人证明重链和轻链的顺序不影响T细胞上抗KDR CAR的表达水平。
此外,细胞可以配备多个单链抗体,从而扩大CAR效应细胞的抗原识别能力。在这里,有多种选择:CARs可以用双元件的载体转导,诱导两个CAR结构的表达;或者将两个单链抗体融合在一个结构中,产生串联单链抗体的“单柄”CAR。虽然这些技术已用于生产CAR-T细胞,但CAR-NK细胞仍未知。
目前大多数临床CAR-T细胞试验都使用了来自小鼠抗体的单链抗体,这增加了抗小鼠IgG细胞宿主抗移植物病的风险,这个问题可以通过人源化或筛选全人抗体避免。然而不幸的是,由于这些CAR受体的嵌合特性,即使是人源化的单链抗体也可能诱导宿主抗独特型免疫反应。幸运的是,在迄今为止数量有限的CAR-NK临床试验中,没有发现与抗CAR免疫反应相关的重大副作用。
连接区
重链和轻链之间的连接区有助于稳定单链抗体的构象,过短会导致多聚体的形成,过长可能导致水解或降低VH和VL结构域之间的关联。对于CAR-NK细胞,五肽GGGGS的多聚体应用为广泛,通常为3个重复。另一个旨在增强蛋白水解稳定性的连接体是Whitlow“218”连接体:GSTGSGSKPGSGEGSTKG。
目前,虽然大多数CAR-NK研究没有提供连接细节,但已有的研究报道中,有22项使用了G4S连接,有2项应用了218连接。
铰链区
铰链区是连接单链抗体单位和跨膜结构域的CAR细胞外结构区,它通常维持效应细胞中稳健的CAR表达和活性所需的稳定性。大多数CAR-NK构建使用CD8α或CD28胞外结构域的衍生物或基于IgG的铰链区。
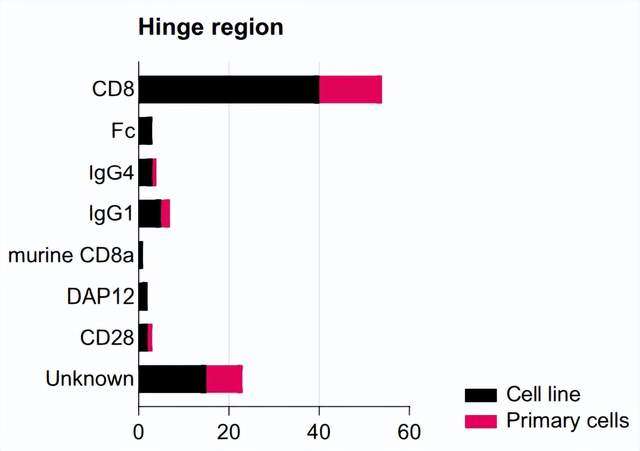
铰链区的类型和长度对CAR的功能活动有重要影响。但是目前大多数信息全来自CAR-T领域,能否直接转化为CAR-NK还有待证明。
在CD28和CD8α铰链区之间的直接比较中,发现CD28更有可能促进CAR分子的二聚化,因此,CD28铰链区的CAR产生的激活刺激更强。虽然这可能是有益的,但也可能导致更严重的副作用。
IgG为基础的铰链区也广泛应用于CAR结构。基于IgG铰链区的一个主要优点是结构的灵活性,该结构通常由IgG1或IgG4的FC部分或Fc部分的CH2/CH3结构域组成。铰链区的长度可以调节以适应抗原识别,但研究发现,间隔区越短,细胞因子的产生越高,CAR-T细胞增殖越快,体内持久性和抗肿瘤效果越好。
对于CAR-NK细胞,大多数研究在原代NK细胞(16/35)和CAR-NK细胞系(41/72)中均采用CD8α铰链区。其它使用的铰链区包括CD28、IgG Fc结构域和DAP12。
跨膜结构域
跨膜(TM)结构域连接CAR的胞外结构域和细胞内激活信号结构域,CAR-NK常用的TM部分来自CD3ζ、CD8和CD28,但其他如NKG2D、2B4、DNAM1也有被使用。
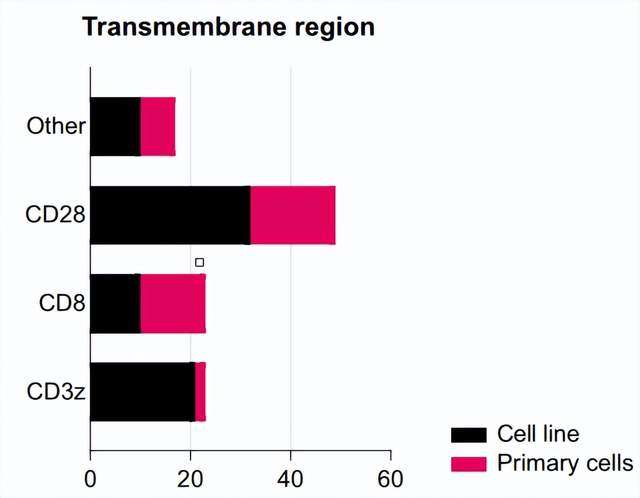
TM结构域的选择影响了CAR结构在细胞功能上的活化程度。通常在NK细胞上表达的分子如DNAM-1、2B4和NKG2D的TM会导致更多的CD107a脱颗粒和更高的细胞毒性,因此,TM的具体来源将决定CAR-NK的活性。
TM结构域的一个重要方面是,佳TM区域应遵循T细胞或NK细胞上跨膜蛋白的蛋白质自然取向(N端到C端顺序)。NKG2D虽然是一种强大的NK细胞激活剂,然而,天然NKG2D具有C端到N端的跨膜区。
目前,CD8α和CD28修饰的TM在原代CAR-NK细胞中常见,而CD28是CAR-NK细胞系的首选TM区域。
CAR-NK激活信号
CAR的细胞内激活信号的数量决定了其属于哪一“代”CAR。
代CAR-NK细胞与CAR-T细胞一样,只含有CD3ζ信号。第二代和第三代CAR-NK分别携带一个和两个额外的共刺激信号,共刺激分子通常来源于CD28家族(CD28和ICOS)、TNFR家族(4-1BB、OX40和CD27)或SLAM相关受体家族(2B4)。到目前为止,唯一公布的CAR-NK临床试验采用了第二代CAR-NK构建,该构建通过加入IL-15表达和诱导Caspase9增强活性。
目前大多数CAR结构依赖于CD3ζ链信号域,强烈的激活信号对于诱导有效的抗肿瘤反应很重要,但也可能导致效应细胞的快速衰竭。因此,共刺激域的组合可用于校准所需的免疫细胞反应。与基于4-1BB的 CARs相比,基于CD28的CARs表现出更快的效应器特征,诱导更高水平的IFN-γ、颗粒酶B、TNF-α。然而,这种强烈的共刺激信号也会导致活化诱导的细胞死亡(AICD)。
相比较,4-1BB-CD3ζ信号优先诱导记忆相关基因和持续的抗肿瘤活性。原因可能是4-1BB结构域改善了CD28结构域引起的T细胞耗竭。
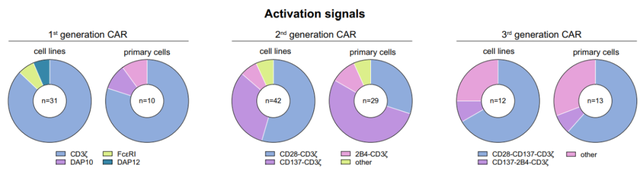
如上图所示,在CAR-NK细胞系和原代CAR-NK细胞的研究中,CD3ζ几乎被普遍用作主要的激活域,其中大约一半携带一个额外的激活域,通常添加4-1BB或CD28。至于第三代结构,CD28/4-1BB/CD3ζ的组合是常用的。
NK细胞定向接合器
各种免疫逃避机制限制了NK细胞在体内与肿瘤细胞的结合程度,是实现广泛有效的NK细胞治疗的主要障碍。为了增强肿瘤浸润性NK细胞的自然细胞毒性,许多研究团队已经在开发一些分子,使这些细胞以抗原特异性的方式与肿瘤细胞接触。这些分子通常是由多个抗体(通常为单链抗体)组成的双特异或三特异性接合器,使得一个结构域针对NK细胞激活受体,另一个与特定肿瘤相关抗原结合。例如,一种由两个单链抗体组成的三特异性杀伤接合器(TriKE),一个针对NK细胞上的CD16,另一个针对AML细胞的CD33,通过IL-15结构域连接,该结构域旨在增强NK细胞的存活和增殖。
这种抗CD16、IL-15和抗CD33 TriKE(GTB-3550)增强了NK细胞效应器功能的其他几个重要方面,在临床前研究中观察到了改善迁移能力、增加连续杀伤和缩短首次杀伤时间。
在临床前研究中,其他几种NKCE分子也被证明具有强大的抗肿瘤作用。AFM13靶向淋巴瘤相关抗原CD30和CD16a,后者是NK细胞表达的CD16的跨膜形式。AFM13在AACR 2022中表现惊艳,AFM13+脐血来源NK细胞治疗,完全缓解率达到62%。
展望
自然杀伤细胞是一组独特的抗肿瘤效应细胞,具有不受MHC限制的细胞毒性、产生细胞因子和免疫记忆等功能,使其成为先天性和适应性免疫反应系统中的关键角色。一些癌症的发生与功能失调的NK细胞有关。因此,修复这种NK细胞可能是抗肿瘤免疫治疗的一个潜在选择。这种修复的一种方法是抑制免疫检查点,即癌细胞通过控制免疫细胞表面的抑制受体进行免疫逃逸。
利用NK细胞与抗体、免疫细胞接合器、CARs和其它检查点抑制剂的组合方法进行试验,这些方法旨在调节抑制检查点和增强抗肿瘤能力。目标是找到一种基于NK细胞的治疗策略,这种策略是安全的,并且具有广泛临床应用所需的确切疗效。
文章来源:生物药学科普
重组C因子与基于LAL的测试方法具有可比性。使用PyroGene 重组C因子产品进行的4种产品内毒素检测时,结果均在可接受范围以内。对于具体产品的方法选择,可以根据产品的性质来进行确定。
赛桥生物致力于实现CGT工业级核心装备的封闭化、自动化、柔性化、 数字化和智能化,加速推动国产替代,已构建设备与耗材能力平台,完成全套工艺模块的开发,包括全封闭自动化血细胞分离、磁珠激活分选、电转染、细胞扩增、清洗浓缩、制剂分装等设备,以及配套的系列化GMP一次性密闭耗材。力争突破进口垄断、为行业客户提供完全国产自主可控的CGT数字化工艺装备平台。
低温样品的移动基站——斯特林 Stirling ULT25NEU 车载便携式超低温冰箱可用于远程临床试验样本采集、实验室小批量样本存储和生物药物配送,为实验室、科研机构生物样品的超低温贮存和运输赋能。
Online Message